L’ANSM publie le rapport d’activité d’hémovigilance 2024
Chaque année, nous publions le bilan des données nationales d’hémovigilance relatives à la surveillance de l’ensemble de la chaîne transfusionnelle (de la collecte de sang au suivi des receveurs).
L’analyse des données 2024 montre que la majorité des effets indésirables survenant chez les receveurs sont non sévères et comparables aux années précédentes.
Depuis le 2 janvier 2024, seuls les effets indésirables graves survenant chez les donneurs de sang sont déclarés au niveau national, comme c’était déjà le cas au niveau européen. Les effets indésirables graves survenant chez les donneurs de sang sont comparables à ceux déclarés les années précédentes et sont en majorité sans conséquence pour le donneur.
Aucun signal n’a été identifié en 2024.
L’hémovigilance est la surveillance, l’évaluation et la prévention des incidents et effets indésirables, survenant chez les donneurs de sang et les receveurs de produits sanguins labiles (PSL). Elle s’applique à l’ensemble de la chaîne transfusionnelle, c’est-à-dire de la collecte des PSL jusqu’au suivi des receveurs.
L'hémovigilance surveille et évalue :
- Les effets indésirables graves survenant chez les donneurs de sang (EIGD) ;
- Les informations post-don (IPD), susceptibles de compromettre la qualité ou la sécurité des produits sanguins issus de ces dons ou de dons antérieurs ;
- Les incidents graves (IG) de la chaîne transfusionnelle, de la collecte des PSL au suivi des receveurs ;
- Les effets indésirables (graves et non graves) survenant chez les receveurs de produits sanguins labiles (EIR).
Les chiffres clés du rapport sur les données 2024
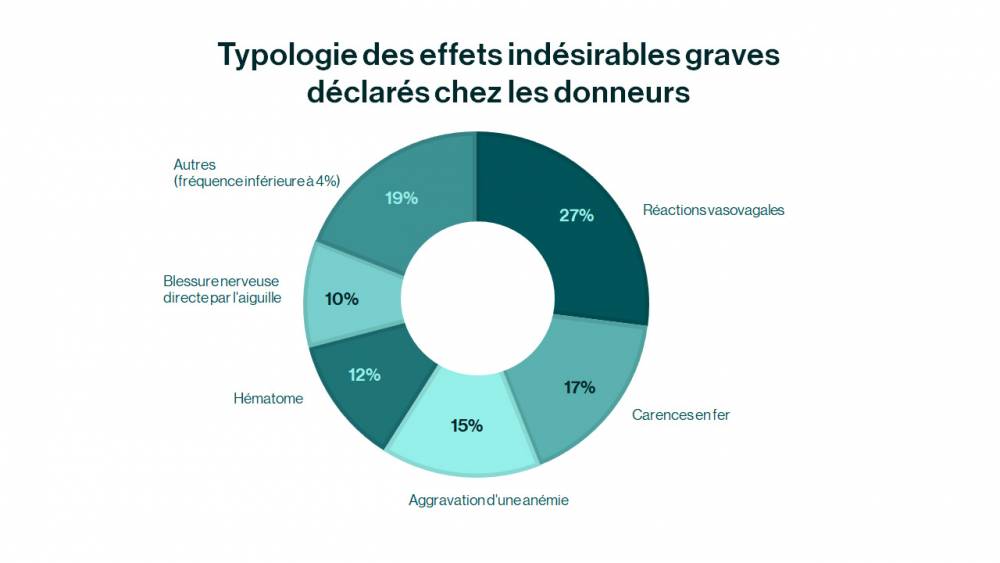
Effets indésirables graves donneurs (EIGD)
En 2024, 115 effets indésirables graves fortement imputables au don ont été déclarés au système d’hémovigilance pour 1 557 675 donneurs.Les effets indésirables graves donneurs (EIGD) sont majoritairement des malaises vagaux (réactions vasovagales), des carences en fer ou encore des aggravations d’une anémie. Dans la majorité des cas, ces EIGD sont sans conséquence pour le donneur ou ont entraîné des arrêts de travail de courte durée.
Le périmètre de déclaration au système national d’hémovigilance des effets indésirables survenant chez les donneurs de sang a été modifié le 2 janvier 2024.
Depuis cette date, les effets indésirables de sévérité modérée (dits de grade 2, comme les malaises vagaux ou des hématomes légers sans signe de gravité) continuent à être recueillis, analysés et suivis par les établissements de transfusion sanguine de l’établissement français du sang (EFS) et du Centre de transfusion sanguine des armées (CTSA) mais ne sont plus déclarés dans le système national, comme c’est le cas au niveau européen. En cas de signal potentiel, les grades 2 sont toutefois analysés par l’ANSM qui peut prendre toute mesure nécessaire.
De même, le périmètre de ces effets a été redéfini en cohérence avec les recommandations européennes.
Cette évolution permet une surveillance homogène de ces effets indésirables graves au niveau européen.
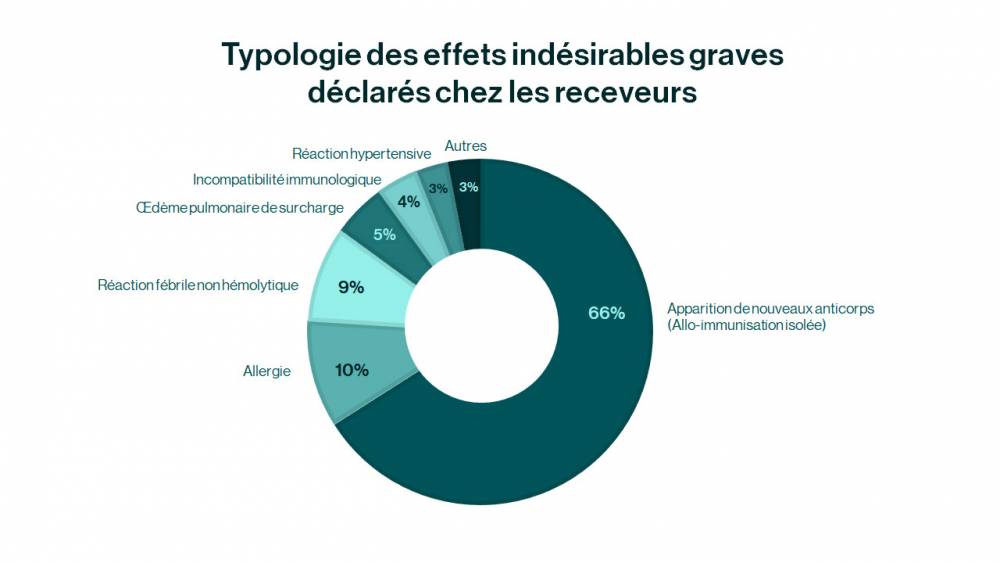
Effets indésirables receveurs (EIR)
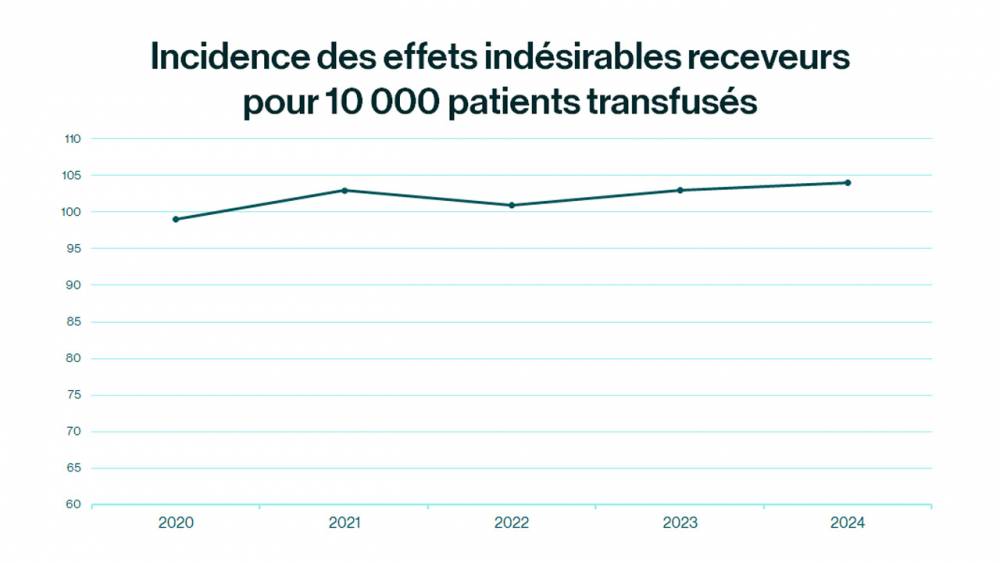
En 2024, 520 872 patients ont été transfusés. Ces transfusions ont donné lieu à la déclaration de 5 431 effets indésirables fortement imputables à la transfusion, en augmentation de 0,4 %.Pour les receveurs, 92 % des effets indésirables fortement imputables à la transfusion sont « non sévères ». Ce sont essentiellement, par ordre de fréquence, des allo-immunisations isolées (dont 99 % de grade 1, la gravité la plus faible), des allergies (dont 73,6 % de grade 1), des réactions fébriles non hémolytiques (dont 97,6 % de grade 1). Les effets indésirables graves (grade 2 à 4) représentent 8 % des effets indésirables imputables à la transfusion. Ce sont essentiellement des effets indésirables connus (allergie, œdème pulmonaire de surcharge, hémolyse retardée chez le drépanocytaire, etc.).
Le taux d’EIR pour 10 000 patients transfusés reste comparable à celui des années précédentes.
Incidents de la chaîne de transfusion
Au total, 2 545 incidents de la chaîne transfusionnelle ont été déclarés. Ils concernent toutes les étapes de la chaîne transfusionnelle, depuis la collecte de sang jusqu’à la transfusion des produits sanguins labiles.- 56% constituent des déclarations de surprélèvement de sang total (incidents non graves).
92 % de ces incidents sont sans conséquence pour les donneurs de sang. Les 8 % signalés avec conséquence pour les donneurs de sang sont de gravité mineure. - 44 % constituent des incidents graves (IG). Pour les IG dont l’enquête est terminée (997), environ 48 % ont une conséquence avérée ou potentielle chez le patient, comme la nécessité d’un prélèvement de contrôle ou l’interruption du protocole transfusionnel. Les IG associés à des effets indésirables chez le receveur (EIR) représentent environ 3 % de l’ensemble des IG dont l’enquête est terminée.
Les IG relatifs à la collecte de sang entraînent des conséquences chez le donneur pour 1 % des déclarations : par exemple, ils ne peuvent plus donner leur sang de manière temporaire ou définitive (contre-indication temporaire ou permanente).
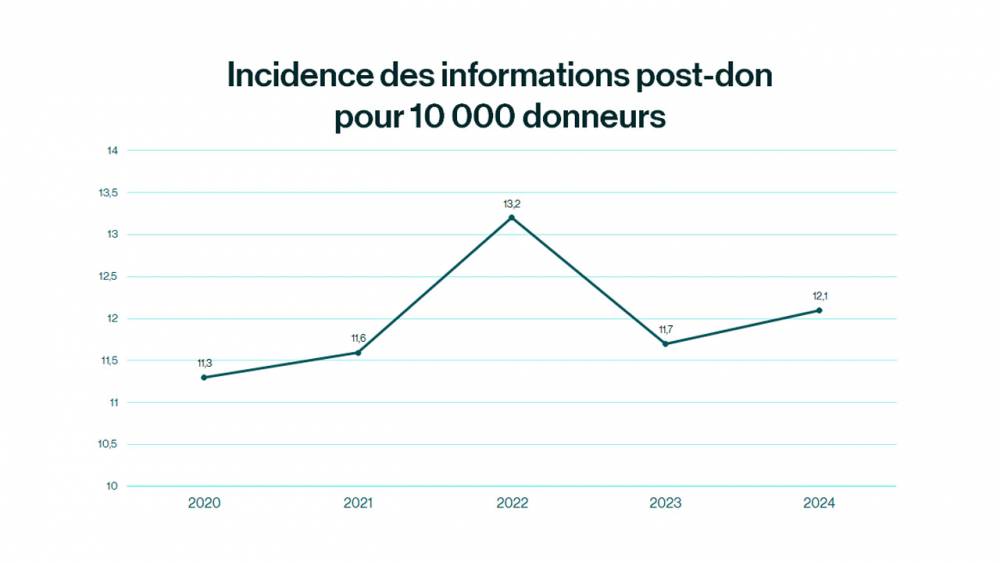
Informations post-don (IPD)
1 880 informations post-don ont été déclarées en 2024. La majorité est de nature infectieuse (90 %).Suivant l’agent infectieux, le donneur ne pourra plus donner son sang de manière temporaire ou définitive. Si nécessaire :
- Les produits issus de ces dons encore en stock à l’établissement de transfusion sanguine sont écartés du circuit thérapeutique transfusionnel ;
- Les prescripteurs des receveurs concernés, pour ceux déjà transfusés, sont prévenus afin de mettre en place un suivi rapproché du patient receveur ;
- Le laboratoire français de fractionnement et des biotechnologies est également prévenu, dans le cas où un plasma lui aurait été envoyé.
Les différents types d’informations post-don
| Infection avérée chez le donneur : 57 % | Exposition du donneur à un risque infectieux : 33 % | Autre risque : 10 % |
|
|
|
- En 2024, une infection bactérienne de grade 3 (impliquant un Staphylococcus ureilyticus) a été transmise par la transfusion (IBTT) d’un concentré de plaquettes d'aphérèse traité pour atténuation des agents pathogènes par amotosalen, et a conduit au décès du patient. Le lien (imputabilité) entre la transfusion et le décès est difficile à évaluer en raison de l’état de santé très dégradé du patient dont le pronostic était défavorable à court terme.
Il n’y a pas eu de risque identifié pour un autre receveur. - Les IBTT restent des évènements rares (1 à 2 cas/an).
- Depuis la généralisation en novembre 2017 de l’inactivation des pathogènes (virus, bactéries, parasites etc.) dans les concentrés plaquettaires (CP), par l’utilisation d’amotosalen puis l’exposition à une lumière UV, 2 autres cas d’IBTT par les CP ont été déjà déclarés (Bacillus cereus).
- Les concentrés de globules rouges (CGR) sont les produits le plus fréquemment impliqués dans la survenue de ces rares cas d’IBTT.
- Les plasmas ne sont pas concernés en raison de leur mode de conservation (congélation à -25 °C). En effet, la conservation des plasmas à des températures très basses permet de ralentir le développement des virus et bactéries et éviter ainsi la transmission de ces agents pathogènes.
- Le nombre d’incidents de la chaîne transfusionnelle de surprélèvements de sang total signalés en 2024 est en légère baisse par rapport à 2023 (-1,8 %).