PUBLIÉ LE 25/10/2018
- MIS À JOUR LE 14/03/2021
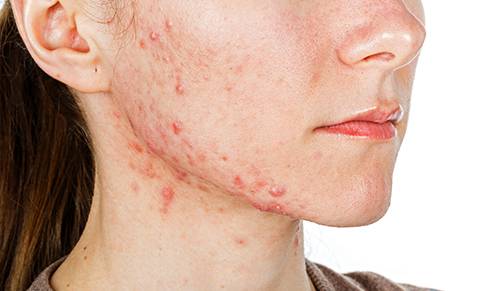
Nouvelle contre-indication pendant la grossesse pour les rétinoïdes utilisés par voie cutanée dans le traitement de l’acné
Les traitements par voie cutanée à base de rétinoïdes (trétinoïne, isotrétinoïne, adapalène, tazarotène), principalement utilisés dans le traitement de l’acné, sont désormais contre-indiqués chez la femme enceinte ou planifiant une grossesse. Les rétinoïdes utilisés par voie orale sont d’ores et déjà contre-indiqués dans cette population et plus largement chez toutes les femmes en âge de procréer sans contraception efficace.
Les médicaments à base de rétinoïdes sont utilisés en dermatologie et cancérologie. Ils sont disponibles sous forme orale (gélule, capsule molle…) ou cutanée (gel, crème…).L’effet tératogène des rétinoïdes par voie orale est connu et la grossesse est une contre-indication absolue lorsqu’ils sont utilisés sous cette forme et de nombreuses mesures de réduction des risques (renforcement des conditions de prescription, documents d’information, formulaire d’accord de soins…) ont déjà été mises en place depuis plusieurs années en France.
Afin d’harmoniser l’information sur les risques de l’ensemble des rétinoïdes, lorsqu’ils sont administrés par voies cutanée ou orale, l’Agence européenne des médicaments (EMA) a conduit un travail de réévaluation de leur rapport bénéfice/risque et a publié ses conclusions en juin 2018.
La principale mesure préconisée par cette réévaluation porte sur le risque tératogène associé aux rétinoïdes administrés par voie cutanée.
En effet, bien qu’un passage dans la circulation sanguine des rétinoïdes à travers la peau semble négligeable dans les conditions habituelles de traitement, il ne peut être totalement exclu. Ainsi, prenant en compte qu’il n’existe pas de besoin absolu pour un traitement rétinoïde par voie cutanée, il a été décidé de contre-indiquer leur utilisation chez la femme enceinte ou planifiant une grossesse.
Par ailleurs, la réévaluation de la sécurité d’emploi des rétinoïdes oraux a conduit à quelques modifications des conditions d’emploi de ces médicaments par rapport aux mesures déjà mises en place en France. De nouveaux outils visant à réduire ces risques sont en cours d’élaboration.
Un courrier informera les professionnels de santé de la mise à disposition de ces documents, prévue en début d’année 2019.
Médicaments commercialisés en France contenant un rétinoïde, par voie cutanée :
- Tretinoine : Zanea, Erylik, Retacnyl, Effederm, Ketrel, Locacid
- Isotretinoine : Antibiotrex, Roaccutane
- Adapalène : Differine, Epiduo, génériques d'adapalène
- Tazarotène : Zorac