Pour rappel
Le Règlement (UE) 2017/745 du Parlement européen et du Conseil du 5 avril 2017 relatif aux dispositifs médicaux, modifiant la directive 2001/83/CE, le règlement (CE) n° 178/2002 et le règlement (CE) n° 1223/2009 et abrogeant les directives du Conseil 90/385/CEE et 93/42/CEE devrait entrer en vigueur en mai 2021.
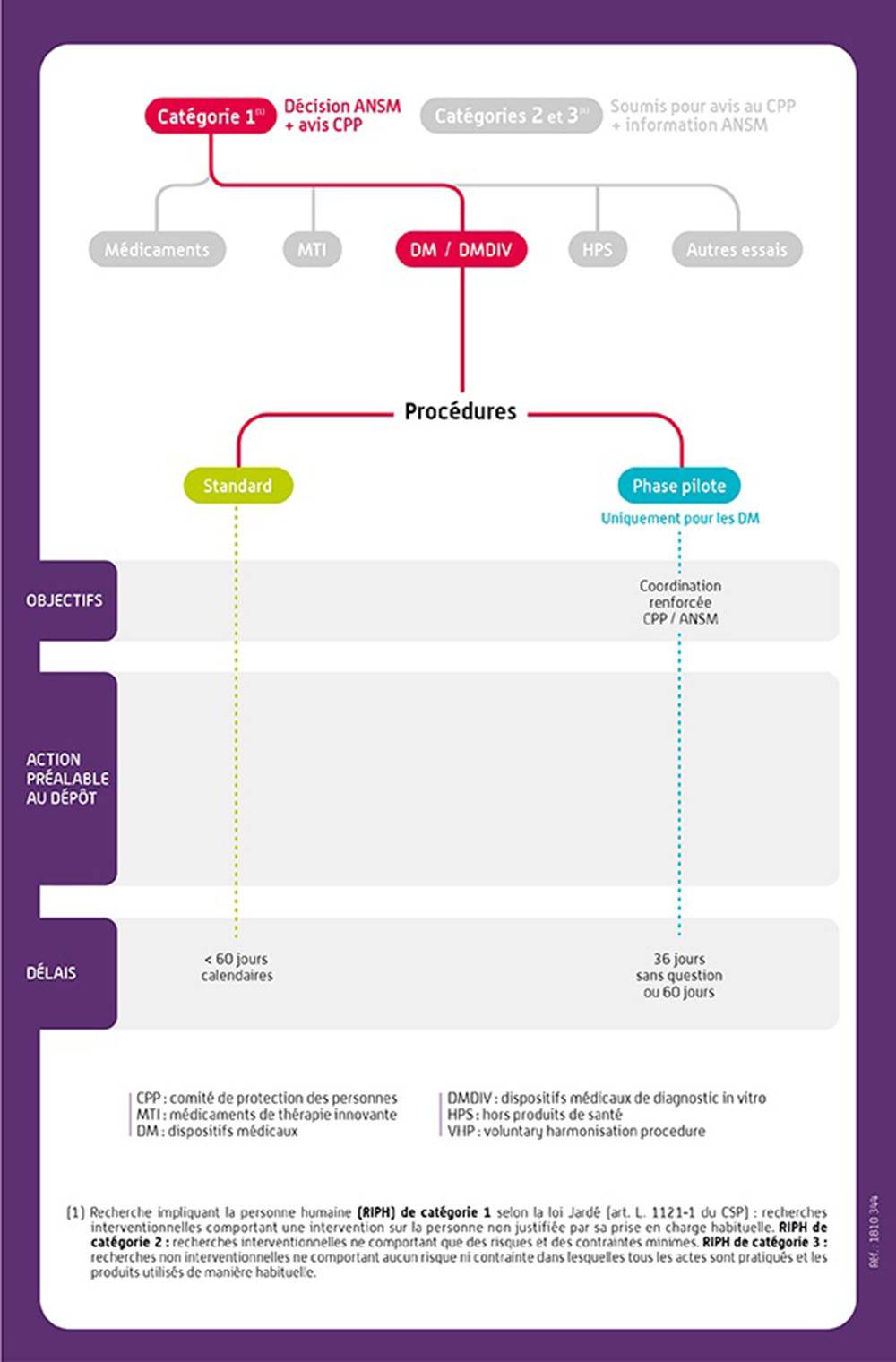
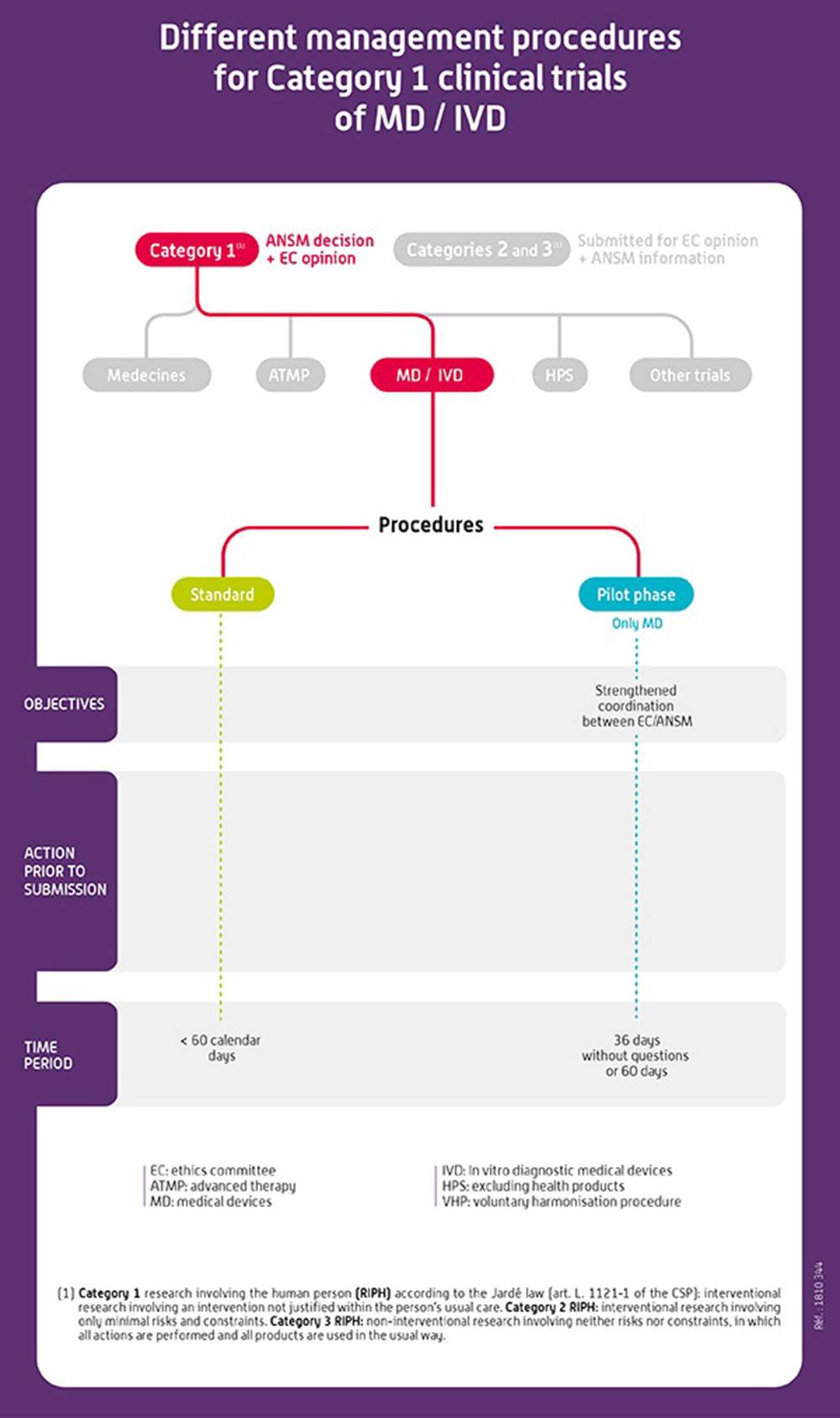
Dans l’attente, les procédures de gestion des demandes d’autorisation d’essais cliniques mises en place ci-après s’appliquent :
Dans l’attente, les procédures de gestion des demandes d’autorisation d’essais cliniques mises en place ci-après s’appliquent :