PUBLIÉ LE 12/11/2024
- MIS À JOUR LE 30/01/2025
L’ANSM publie son rapport d’hémovigilance de l’année 2023
| Actualisation du 30/01/2025 Correction du rapport d'hémovigilance |
Chaque année, nous publions le bilan des données nationales d’hémovigilance relatives à la surveillance de l’ensemble de la chaîne transfusionnelle (de la collecte de sang au suivi des receveurs). Leur analyse montre que la majorité des effets indésirables, chez les receveurs comme chez les donneurs, sont non sévères et comparables aux années précédentes. Aucun signal n’a été identifié en 2023.
L’hémovigilance est la surveillance, l’évaluation et la prévention des incidents et effets indésirables, survenant chez les donneurs et les receveurs de produits sanguins labiles (PSL). Elle s’applique à l’ensemble de la chaîne transfusionnelle, c’est-à-dire de la collecte des PSL jusqu’au suivi des receveurs.L'hémovigilance surveille et évalue:
- Les effets indésirables survenant chez les donneurs de sang (EIGD) ;
- Les informations post-don (IPD), susceptibles de compromettre la qualité ou la sécurité des produits sanguins issus de ces dons ou de dons antérieurs ;
- Les incidents de la chaine transfusionnelle, de la collecte des PSL au suivi des receveurs ;
- Les effets indésirables survenant chez les receveurs de produits sanguins labiles (EIR).
En savoir plus sur l’hémovigilance et son organisation
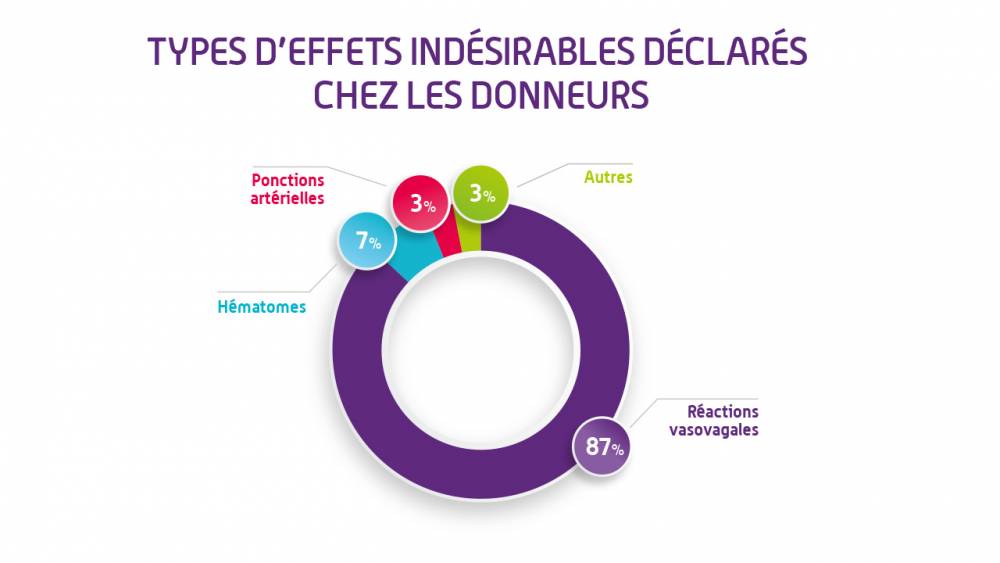
Les effets indésirables chez les donneurs de sang (EIGD) sont sans conséquence pour le donneur dans près de 96% des cas et très majoritairement de gravité modérée (77 %). Avec 87 % des déclarations, le malaise vagal est l’effet indésirable le plus fréquemment rapporté. Les réactions locales (hématome (bleu), ponction artérielle, etc.) constituent le second effet en termes de fréquence.
Suivant l’agent infectieux, le donneur est alors contre-indiqué au don, temporairement ou définitivement. Si nécessaire :
Suite aux retours (non exhaustifs) des enquêtes réalisées auprès des patients transfusés avec un produit sanguin issu d’un don à risque (objet d’une IPD), 7 EIR ont été déclarés, dont 6 infections par le virus de l’hépatite E (VHE).
Les IBTT restent des évènements rares (1 à 2 cas/an). Depuis la généralisation en novembre 2017 de l’inactivation des pathogènes (virus, bactéries, parasites etc.) par le procédé Intercept dans les concentrés plaquettaires (CP) (i.e. traités par l’Amotosalen), seulement 2 cas d’IBTT par les CP ont été déclarés (Bacillus cereus). Les concentrés de globules rouges (CGR) sont les produits le plus fréquemment impliqués dans la survenue de ces rares cas d’IBTT. Les plasmas ne sont pas concernés en raison de leur mode de conservation (congélation à -25 °C). Il n’y a eu ni complication ni séquelle pour ces patients et il n’y a pas eu de risque identifié pour un autre receveur.
Le nombre d’incidents de la chaîne transfusionnelle de surprélèvements de sang total signalés en 2023 est en légère baisse par rapport à 2022 (-2,3 %).
Les erreurs de patients destinataires de produits sanguins labiles (PSL) sont en baisse. 61 % de ces incidents ont eu une conséquence pour les patients transfusés (retard de soin, nécessité de prélèvement de contrôle). Le respect des dispositions de l’instruction du 16 novembre 2021 relative à l’acte transfusionnel doit permettre de réduire la survenue de cet incident évitable.
Suite à l'identification d'une erreur dans le calcul de l'incidence des décès fortement imputables à la transfusion, le rapport publié le 12 novembre 2024 a été modifié :
En 2023, le taux d’incidence des décès fortement liés à la transfusion (incluant les 2 grades 4 imputabilité probable) est de 0,14 EIR (et non pas 0,5) pour 100 000 PSL cédés, de 0,15 EIR (et non pas 0,6) pour 100 000 PSL transfusés et de 0,08 (et non pas 0,3) EIR pour 10 000 patients transfusés.
Consultez le nouveau rapport :
Les chiffres clés du rapport sur les données 2023
Effets indésirables donneurs (EIGD)
7 723 effets indésirables fortement imputables au don ont été déclarés au système d’hémovigilance pour 1 547 679 donneurs.Les effets indésirables chez les donneurs de sang (EIGD) sont sans conséquence pour le donneur dans près de 96% des cas et très majoritairement de gravité modérée (77 %). Avec 87 % des déclarations, le malaise vagal est l’effet indésirable le plus fréquemment rapporté. Les réactions locales (hématome (bleu), ponction artérielle, etc.) constituent le second effet en termes de fréquence.
Les autres EIGD imputables au don sont rares : leur fréquence respective est inférieure à 1 %. Pour les effets indésirables les plus graves (c’est-à-dire ceux qui donnent lieu à un traitement médical à la collecte ou à une consultation médicale), on observe un rétablissement complet dans la majorité des cas.
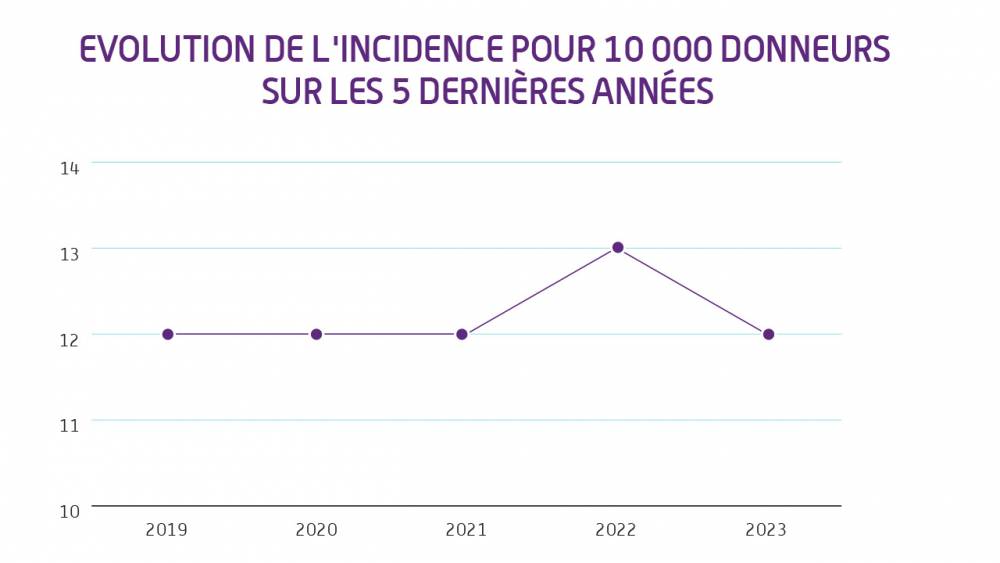
Les effets indésirables déclarés chez les donneurs de sang (EIGD) ont augmenté de 15,1 % alors que les prélèvements ont diminué de 2,1 % par rapport à 2022. Le taux d’EIGD pour 100 000 prélèvements est en augmentation par rapport à l’année précédente.
Cette augmentation pourrait s’expliquer par plusieurs facteurs : une meilleure sensibilisation des donneurs au signalement des EIGD, une augmentation des prélèvements d’aphérèse (car l’incidence des EIGD est supérieure pour les dons d’aphérèse par rapport aux dons de sang total), ou encore une évolution du profil des donneurs. Le nombre de donneurs de la tranche d'âge 18-19 ans a ainsi augmenté de 2,8% par rapport à 2022 et le nombre de primo-donneurs âgés de 18 à 24 ans de 2,1% par rapport à 2022, or l’incidence des EIGD est supérieure pour les tranches d’âge les plus jeunes et pour les primo-donneurs.
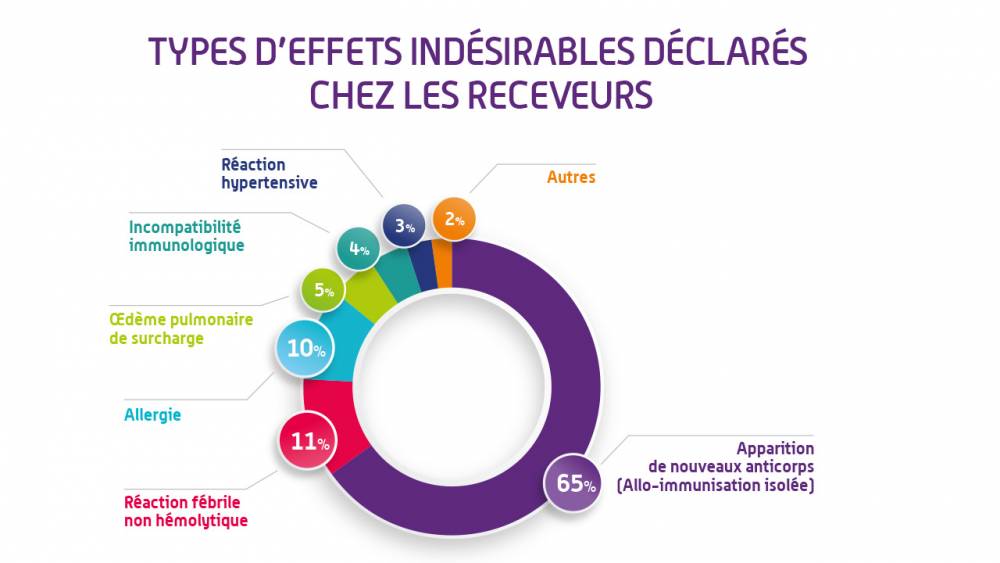
Pour les receveurs, 92 % des effets indésirables imputables à la transfusion (imputabilité probable ou certaine) sont non sévères. Ce sont essentiellement, par ordre de fréquence, des allo-immunisations isolées (dont 99,5 % de grade 1, la gravité la plus faible), des réactions fébriles non hémolytiques (dont 97,2 % de grade 1) et des allergies (dont 73,3 % de grade 1). Les effets indésirables graves (grade 2 à 4) représentent 8 % des effets indésirables imputables à la transfusion. Ce sont essentiellement des effets indésirables connus (allergie, œdème pulmonaire de surcharge, hémolyse retardée chez le drépanocytaire, etc.).
Les effets indésirables déclarés chez les donneurs de sang (EIGD) ont augmenté de 15,1 % alors que les prélèvements ont diminué de 2,1 % par rapport à 2022. Le taux d’EIGD pour 100 000 prélèvements est en augmentation par rapport à l’année précédente.
Cette augmentation pourrait s’expliquer par plusieurs facteurs : une meilleure sensibilisation des donneurs au signalement des EIGD, une augmentation des prélèvements d’aphérèse (car l’incidence des EIGD est supérieure pour les dons d’aphérèse par rapport aux dons de sang total), ou encore une évolution du profil des donneurs. Le nombre de donneurs de la tranche d'âge 18-19 ans a ainsi augmenté de 2,8% par rapport à 2022 et le nombre de primo-donneurs âgés de 18 à 24 ans de 2,1% par rapport à 2022, or l’incidence des EIGD est supérieure pour les tranches d’âge les plus jeunes et pour les primo-donneurs.
Effets indésirables receveurs (EIR)
En 2023, 524 196 patients ont été transfusés. Ces transfusions ont donné lieu à la déclaration de 5 412 effets indésirables fortement imputables à la transfusion, en augmentation de 1,5 %.Pour les receveurs, 92 % des effets indésirables imputables à la transfusion (imputabilité probable ou certaine) sont non sévères. Ce sont essentiellement, par ordre de fréquence, des allo-immunisations isolées (dont 99,5 % de grade 1, la gravité la plus faible), des réactions fébriles non hémolytiques (dont 97,2 % de grade 1) et des allergies (dont 73,3 % de grade 1). Les effets indésirables graves (grade 2 à 4) représentent 8 % des effets indésirables imputables à la transfusion. Ce sont essentiellement des effets indésirables connus (allergie, œdème pulmonaire de surcharge, hémolyse retardée chez le drépanocytaire, etc.).
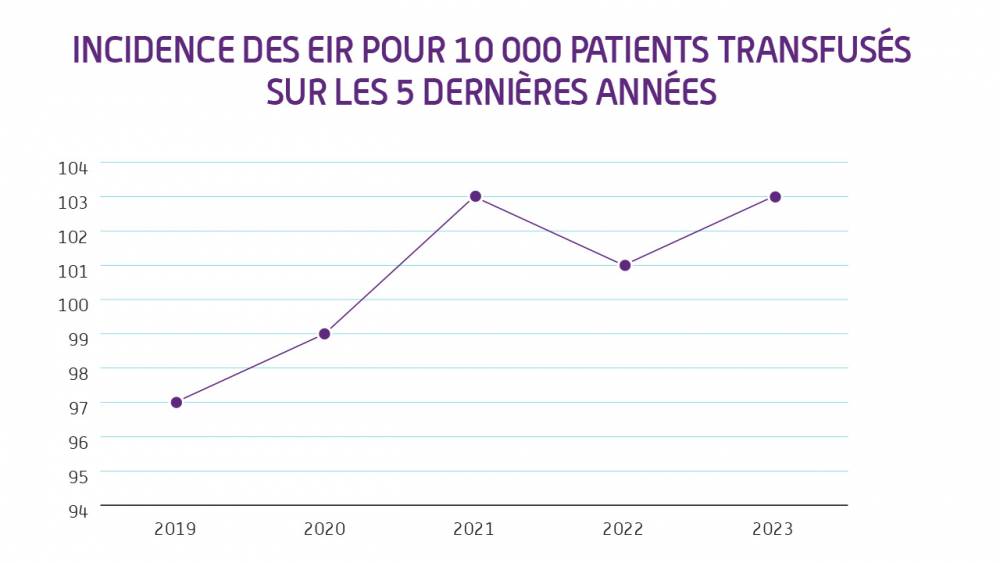
Le taux d’EIR pour 10 000 patients transfusés reste comparable à celui des années précédentes.
Incidents de la chaîne de transfusion
Au total, 2 613 incidents de la chaîne transfusionnelle ont été déclarés. Ils concernent toutes les étapes de la chaîne transfusionnelle, depuis la collecte de sang jusqu’à la transfusion des produits sanguins labiles.- 56% constituent des déclarations de sur-prélèvements de sang total (incidents non-graves).
- 91 % de ces incidents sont sans conséquence pour les donneurs de sang. Parmi les 9 % signalés avec conséquence pour les donneurs de sang, 85 % sont de gravité mineure. Les 15 % restants (20 EIGD) sont de gravité modérée (n=17) à sévère (n=3) de type réaction vasovagale
- 44 % constituent des incidents graves (IG).Pour les IG dont l’enquête est terminée (996), environ 57 % ont une conséquence avérée ou potentielle chez le patient, comme la nécessité de prélèvement de contrôle, l’interruption du protocole transfusionnel. Les IG associés à des effets indésirables chez le receveur (EIR) représentent in fine environ 4 % de l’ensemble des IG en enquête terminée.
Les IG relatifs à la collecte de sang sont associés à des conséquences chez le donneur pour 2% des déclarations, comme une contre-indication temporaire ou permanente au don du sang.
Information post-don (IPD)
1 805 informations post-don ont été réalisées en 2023. La majorité est de nature infectieuse (90 %).Suivant l’agent infectieux, le donneur est alors contre-indiqué au don, temporairement ou définitivement. Si nécessaire :
- Les produits issus de ces dons encore en stock à l’établissement de transfusion sanguine sont écartés du circuit thérapeutique transfusionnel ;
- Les prescripteurs des receveurs concernés, pour ceux déjà transfusés, sont prévenus afin de mettre en place un suivi rapproché du patient receveur ;
- Le laboratoire français de fractionnement et des biotechnologies est également prévenu, dans le cas où un plasma lui aurait été envoyé.
Les différentes informations post-don
| Infection avérée chez le donneur : 53 % | Exposition du donneur à un risque infectieux : 37 % | Autre risque : 10 % |
|
|
|
Faits marquants 2023
En 2023, 3 infections bactériennes ont été transmises par la transfusion (IBTT) de concentrés de globules rouges dans 2 cas et d’un mélange de concentrés de plaquettes traité pour inactivation des agents pathogènes pour le 3e cas.Les IBTT restent des évènements rares (1 à 2 cas/an). Depuis la généralisation en novembre 2017 de l’inactivation des pathogènes (virus, bactéries, parasites etc.) par le procédé Intercept dans les concentrés plaquettaires (CP) (i.e. traités par l’Amotosalen), seulement 2 cas d’IBTT par les CP ont été déclarés (Bacillus cereus). Les concentrés de globules rouges (CGR) sont les produits le plus fréquemment impliqués dans la survenue de ces rares cas d’IBTT. Les plasmas ne sont pas concernés en raison de leur mode de conservation (congélation à -25 °C). Il n’y a eu ni complication ni séquelle pour ces patients et il n’y a pas eu de risque identifié pour un autre receveur.
Le nombre d’incidents de la chaîne transfusionnelle de surprélèvements de sang total signalés en 2023 est en légère baisse par rapport à 2022 (-2,3 %).
Les erreurs de patients destinataires de produits sanguins labiles (PSL) sont en baisse. 61 % de ces incidents ont eu une conséquence pour les patients transfusés (retard de soin, nécessité de prélèvement de contrôle). Le respect des dispositions de l’instruction du 16 novembre 2021 relative à l’acte transfusionnel doit permettre de réduire la survenue de cet incident évitable.
Suite à l'identification d'une erreur dans le calcul de l'incidence des décès fortement imputables à la transfusion, le rapport publié le 12 novembre 2024 a été modifié :
En 2023, le taux d’incidence des décès fortement liés à la transfusion (incluant les 2 grades 4 imputabilité probable) est de 0,14 EIR (et non pas 0,5) pour 100 000 PSL cédés, de 0,15 EIR (et non pas 0,6) pour 100 000 PSL transfusés et de 0,08 (et non pas 0,3) EIR pour 10 000 patients transfusés.
Consultez le nouveau rapport :