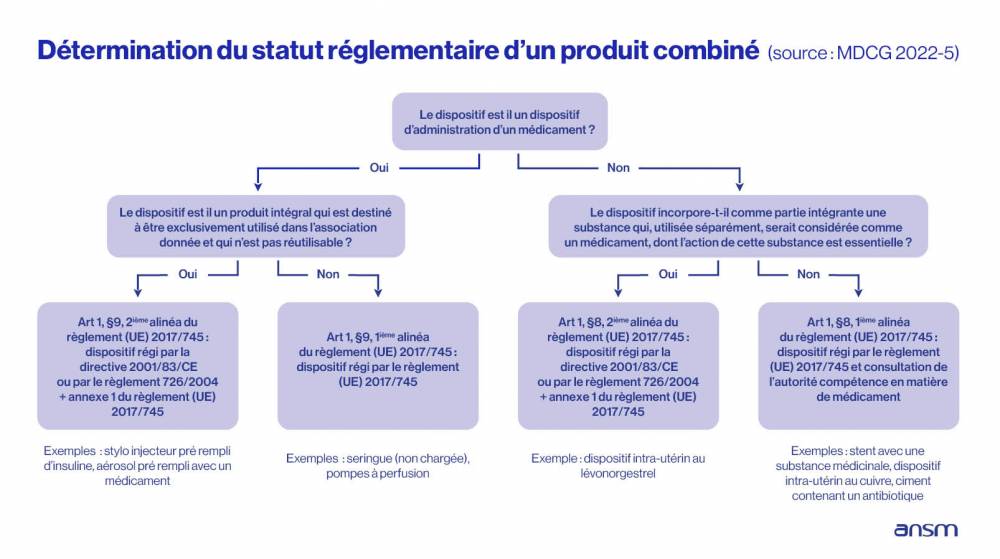
Il est possible de rencontrer sur le marché des dispositifs médicaux combinés avec un médicament et vice versa. On parle alors de produits intégraux. Ce sont soit des dispositifs incorporant comme partie intégrante une substance qui utilisée séparément serait considérée comme un médicament et dont l’action est accessoire à celle du dispositif, soit un dispositif d’administration d’un médicament qui forme un produit intégral unique avec ce médicament et qui est destiné à être utilisé exclusivement dans cette association et qui n’est pas réutilisable. Ces produits sont décrits dans la règlementation européenne de 2017 (article 1er point 8, second alinéa et article 1er point 9, second alinéa).
Le logigramme ci-dessous décrit les étapes permettant de déterminer le statut de produits combinés :
Le logigramme ci-dessous décrit les étapes permettant de déterminer le statut de produits combinés :