Evaluation de la pertinence et de la faisabilité de la mise à disposition du cannabis médical en France
Qu’est-ce qu’une expérimentation ?
Une expérimentation permet de tester, dans des conditions réelles, la mise en place d’une nouvelle politique publique. Elle évalue des solutions sur le terrain, durant un temps limité, afin d’en mesurer les effets et favoriser une prise de décision. L’expérimentation est ainsi différente d’un essai clinique.Pour que l’on puisse parler d’expérimentation, 3 conditions doivent être réunies :
- Il faut définir un objectif et une hypothèse que l’on cherche à valider ;
- L’expérimentation doit avoir un caractère temporaire ;
- Elle doit s’accompagner d’une évaluation dont les conclusions doivent permettre d’éclairer la décision publique qui permettra, le cas échéant, une généralisation.
Historique de la mise en place de l’expérimentation
Mise en place du comité scientifique
Trois facteurs principaux sont à l’origine de la réflexion de l’ANSM sur la faisabilité de la mise à disposition du cannabis médical en France :- Des données scientifiques convergentes qui montraient un intérêt du cannabis dans le traitement de certains symptômes de différentes pathologies ;
- Une demande grandissante de patients et de professionnels de santé ;
- L’usage médical du cannabis dans de nombreux pays en Europe et dans le monde (Pays-Bas, Allemagne, Royaume-Uni, Portugal, Luxembourg, Lituanie, Canada, Israël, Chili, Colombie, et alors 33 Etats aux Etats-Unis).
En décembre 2018, ce comité estimait qu’il était pertinent d’autoriser l’usage médical du cannabis pour les patients dans certaines situations cliniques et a souhaité que soit mise en place une expérimentation.
À partir de janvier 2019, un autre comité (CSST) devait définir les modalités de l’expérimentation et un cadre permettant de sécuriser sa mise en place.
Ce comité devait définir des cahiers des charges pour :
- Les médicaments utilisés durant l’expérimentation ;
- Le contenu de la formation destinée aux médecins et pharmaciens et le contenu de l’information aux patients ;
- Le contenu du registre de suivi des patients.
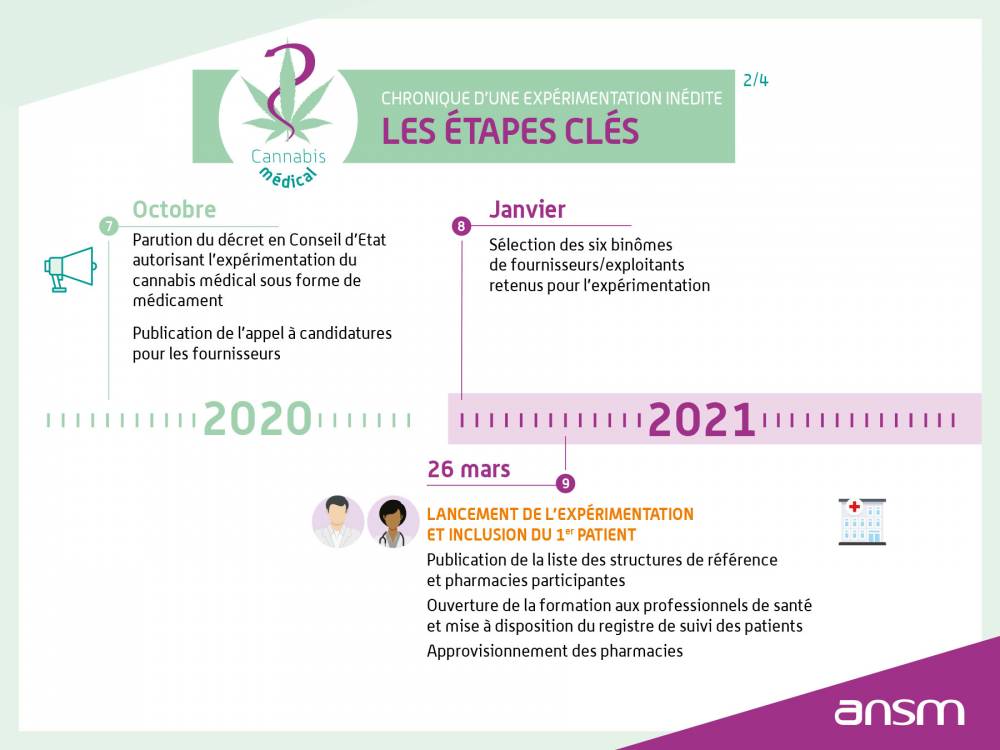
Lancement de l’expérimentation
Le 25 octobre 2019, l'Assemblée nationale donnait son feu vert à une expérimentation de l'usage du cannabis médical dans le cadre de l'examen du projet de budget de la Sécurité sociale pour 2020.Initialement autorisée pour 2 ans en application de l’article 43 de la loi n°2019-1446 du 24 décembre 2019 de financement de la Sécurité sociale pour 2020, cette expérimentation a été prolongée d’une année par l’article 57 de la loi n°2022-1616 du 23 décembre 2022 de financement de la Sécurité sociale pour 2023. Un rapport au Parlement est prévu 6 mois avant la fin de l'expérimentation afin d'envisager les suites pouvant être données à cette expérimentation.
Ainsi, le premier patient a été inclus le 26 mars 2021.
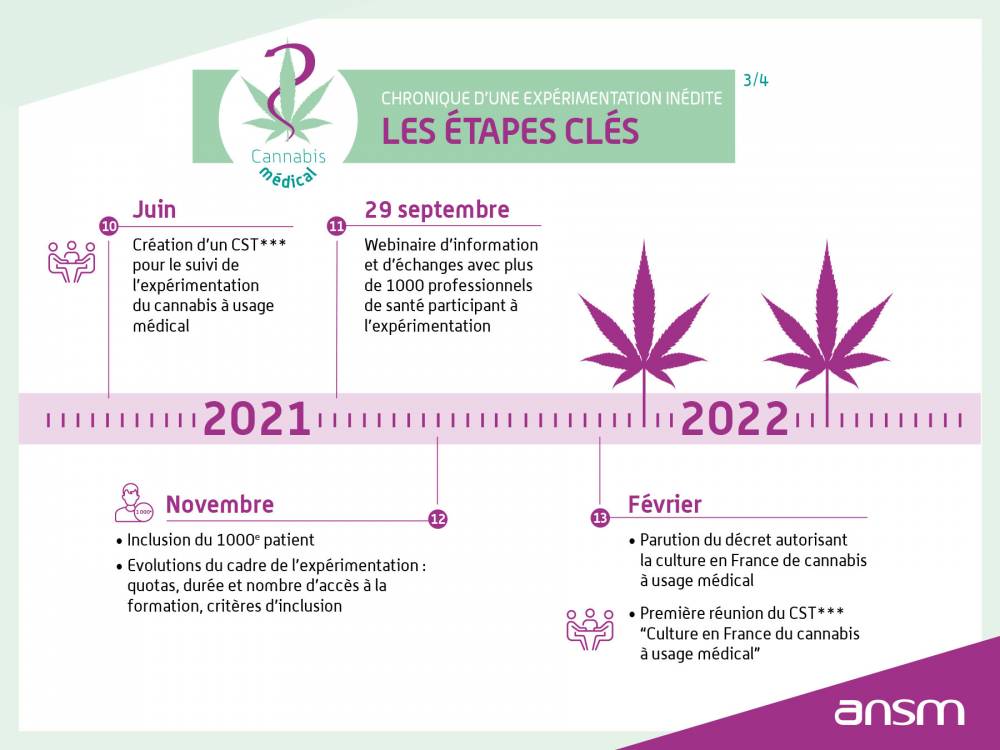
Nos travaux se poursuivent tout au long de l’expérimentation. Le comité scientifique temporaire pour le suivi de l’expérimentation du cannabis à usage médical a été créé en juin 2021. Composé de 16 membres, dont 4 patients et des professionnels de santé, médecins généralistes, spécialistes des indications thérapeutiques retenues pour le cannabis médical, pharmaciens et représentants des Centre régionaux de pharmacovigilance et des Centres d’évaluation et d’information sur la pharmacodépendance-addictovigilance, ce comité participe à la surveillance du déroulement de l’expérimentation et rendra un avis sur les données d’évaluation recueillies et sur l’encadrement de la mise sur le marché et de l’utilisation du cannabis médical.
Une large concertation
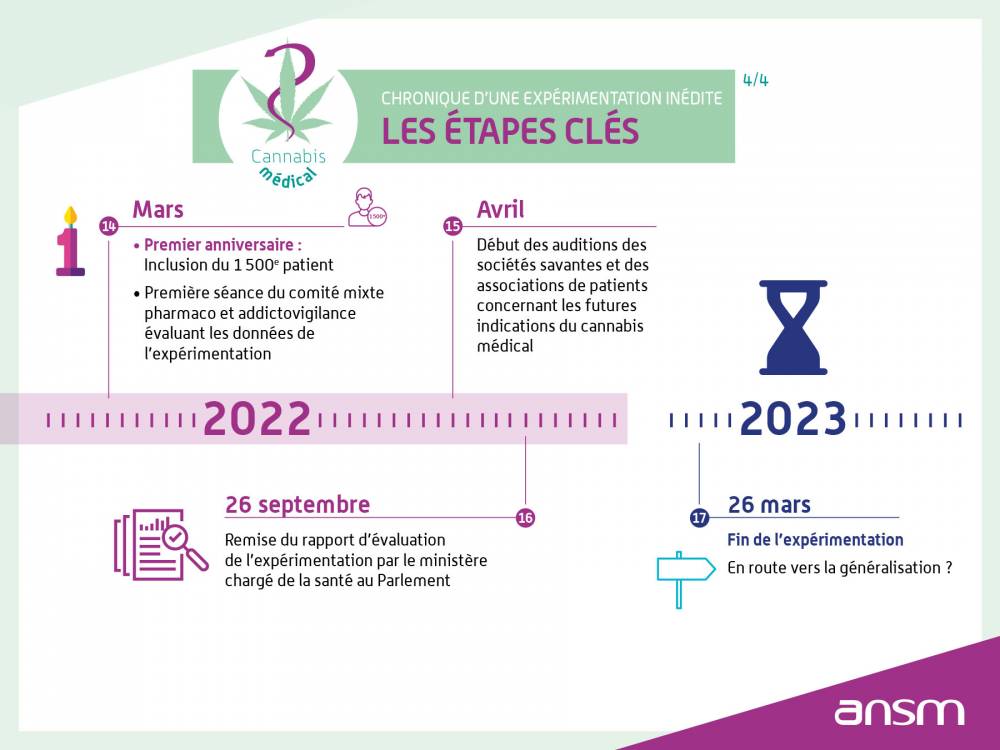
Dans le cadre des différentes réflexions en lien avec l’expérimentation, nous avons consulté, et continuons de consulter associations de patients, professionnels de santé, sociétés savantes, mais également représentants de pays où le cannabis médical est déjà utilisé et acteurs de la filière économique.Fin de l’expérimentation
Les données récoltées lors des 2 premières années de l’expérimentation ont montré un circuit de distribution sécurisé et opérationnel, une efficacité du cannabis dans les indications de l’expérimentation, maintenue sur plusieurs mois chez certains patients, ainsi qu’un profil de sécurité attendu et rassurant avec peu d’effets indésirables graves.L'expérimentation a ensuite été prolongée jusqu'au 31 décembre 2024. Cette prolongation a assuré la continuité de traitement pour les patients déjà inclus au 26 mars 2024. Après cette date, aucun nouveau patient n’est plus rentré dans l’expérimentation.
L’expérimentation a pris fin le 31 décembre 2024. En effet, les travaux parlementaires dans le cadre du projet de loi de financement de la sécurité sociale pour 2025 n’ont pu permettre d’aboutir à une prolongation de cette expérimentation entraînant l’arrêt du dispositif.
Concernant les suites de l’expérimentation et le traitement des patients inclus : l’inclusion des patients dans l’expérimentation a pris fin le 27 mars 2024. Dans l’attente de l’aboutissement des travaux permettant la généralisation du cannabis médical, le ministère a décidé la prolongation de la prise en charge des patients encore sous traitement depuis la fin de l’expérimentation le 31 décembre 2024.
Cette phase transitoire a de nouveau été prolongée par le ministère de la santé afin d’« éviter toute interruption de traitement pour les patients encore pris en charge dans ce cadre transitoire, dans l’attente de la mise en place d’un cadre. »
Elle prendra fin 3 mois après la publication par la Haute Autorité de santé (HAS) de son avis sur son site.
Jusque-là, la prise en charge des patients inclus dans l’expérimentation et encore sous traitement sera assurée dans les mêmes conditions que précédemment et à titre exceptionnel avec les médicaments autorisés pour l’expérimentation.
Travaux pour l’accès généralisé aux médicaments à base de cannabis
La loi de financement de la sécurité sociale (LFSS) pour 2024 prévoyait pour les médicaments à base de cannabis l’octroi d'une autorisation d'utilisation pour une période temporaire de 5 ans, délivrée par l'ANSM.Le ministère chargé de la Santé et de l’Accès aux soins a annoncé le 20 mars dernier que les textes définissant le cadre de production et d’autorisation du cannabis à usage médical ont été notifiés à la Commission européenne. Les trois textes notifiés portent respectivement sur :
- Le cadre du futur dispositif (demande d’autorisation, évaluation, pharmacovigilance, circuit etc.) ;
- Les critères de qualité et de sécurité des médicaments à base de cannabis ;
- Les modalités de culture du cannabis à usage médical sur le territoire national.
En parallèle, la Haute Autorité de santé (HAS) a été saisie par le ministère afin d'évaluer l'intérêt thérapeutique du cannabis médical. Son avis, attendu dans les prochains mois, déterminera si ces médicaments pourront être pris en charge par l'Assurance maladie et à quel taux.